Поняття твердого тіла та його загальні властивості. Кристали.
Кристаллическими считаются вещества, атомы которых расположены в строго определенном порядке, так что образуют правильную трёхмерную решётку, называемую кристаллической.
 Главным отличием кристаллов от других твёрдых тел является наличие кристаллической решётки – совокупности периодически расположенных атомов, молекул или ионов. Главным отличием кристаллов от других твёрдых тел является наличие кристаллической решётки – совокупности периодически расположенных атомов, молекул или ионов.
Русский учёный Е.С.Фёдоров установил, что в природе может существовать только 230 различных пространственных групп, охватывающих все возможные кристаллические структуры. Большинство из них (но не все) обнаружены в природе или созданы искусственно.
Кристаллы могут иметь форму различных призм, основанием которых могут быть правильный треугольник, квадрат, параллелограмм и шестиугольник.
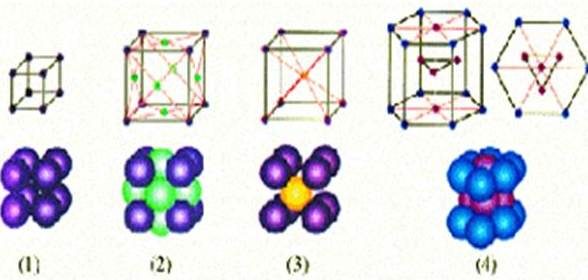 Примеры простых кристаллических решёток: 1 – простая кубическая; 2 – гранецентрированная кубическая; 3 – объёмно-центрированная кубическая; 4 – гексагональная Кристаллические решётки металлов часто имеют форму гранецентрированного (медь, золото) или объёмно-центрированного куба (железо), а также шестигранной призмы (цинк, магний). В основе классификации кристаллов и объяснения их физических свойств может лежать не только форма элементарной ячейки Примеры простых кристаллических решёток: 1 – простая кубическая; 2 – гранецентрированная кубическая; 3 – объёмно-центрированная кубическая; 4 – гексагональная Кристаллические решётки металлов часто имеют форму гранецентрированного (медь, золото) или объёмно-центрированного куба (железо), а также шестигранной призмы (цинк, магний). В основе классификации кристаллов и объяснения их физических свойств может лежать не только форма элементарной ячейки
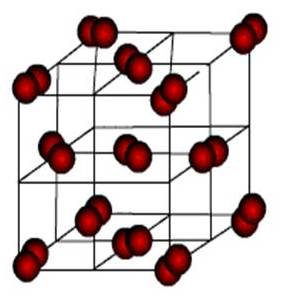
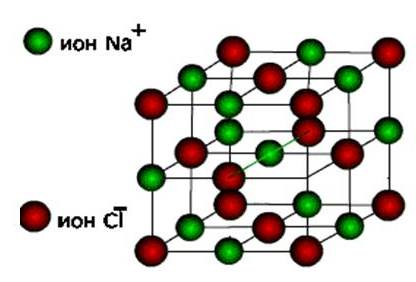 Ионными называют кристаллические решетки, в узлах которых находятся ионы. Их образуют вещества с ионной связью. Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов. Рассмотрим строение кристалла поваренной соли, в узлах которого находятся ионы хлора и натрия. Ионными называют кристаллические решетки, в узлах которых находятся ионы. Их образуют вещества с ионной связью. Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов. Рассмотрим строение кристалла поваренной соли, в узлах которого находятся ионы хлора и натрия.
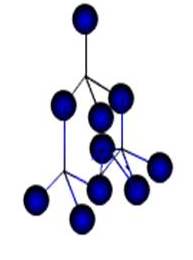 Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы, которые соединены очень прочными ковалентными связями. На рисунке показана кристаллическая решётка алмаза. Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы, которые соединены очень прочными ковалентными связями. На рисунке показана кристаллическая решётка алмаза.
 Молекулярными называют кристаллические решётки, в узлах которых располагаются молекулы. Химические связи в них ковалентные, как полярные, так и неполярные. Связи в молекулах прочные, но между молекулами связи не прочные Молекулярными называют кристаллические решётки, в узлах которых располагаются молекулы. Химические связи в них ковалентные, как полярные, так и неполярные. Связи в молекулах прочные, но между молекулами связи не прочные
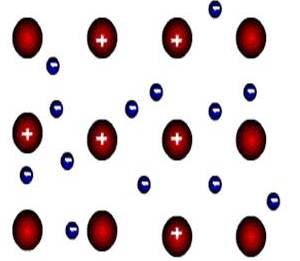 Металлическими называют решётки, в узлах которых находятся атомы и ионы металла. Металлическими называют решётки, в узлах которых находятся атомы и ионы металла. Но не только правильная форма является следствием четкого положения атомов и молекул кристалла в пространстве.
Физические свойства в кристаллах зависят от направления в кристалле —анизотропия. Например, в одном направлении слюда расслаивается, а в другом нет
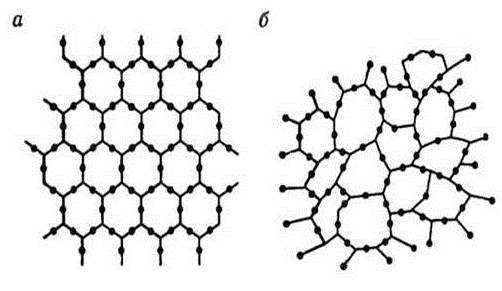 Аморфные тела — это стекло, смола, канифоль, многие пластмассы, сургуч, пластическая сера, янтарь, различные полимеры — органические аморфные тела (целлюлоза, каучук, кожа, плексиглас, полиэтилен) и др. Аморфные тела — это стекло, смола, канифоль, многие пластмассы, сургуч, пластическая сера, янтарь, различные полимеры — органические аморфные тела (целлюлоза, каучук, кожа, плексиглас, полиэтилен) и др. У аморфных тел нет кристаллической решетки, у них обнаружен только ближний порядок в расположении молекул. На рисунке изображена плоская схема расположения молекул кварца (а) и кварцевого стекла — аморфного тела (б).
Аморфное тело обладает слабо выраженной текучестью. Так, если воронку наполнить кусочками воска, то через некоторое время (различное для разных температур) кусочки воска будут "расплываться". Воск примет форму воронки и начнет "вытекать" из нее.
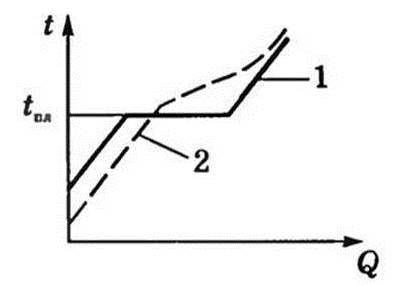 Текучесть связана с перескоками молекул из одного положения равновесия в другое. У аморфных тел нет определенной температуры плавления. Вещество в аморфном состоянии при нагревании постепенно размягчается и переходит в жидкость (кривая 2). Вместо температуры плавления приходится говорить о температурном интервале размягчения. Текучесть связана с перескоками молекул из одного положения равновесия в другое. У аморфных тел нет определенной температуры плавления. Вещество в аморфном состоянии при нагревании постепенно размягчается и переходит в жидкость (кривая 2). Вместо температуры плавления приходится говорить о температурном интервале размягчения. Аморфные тела изотропны, т.е. их физические свойства по всем направлениям одинаковы. Внутренняя энергия вещества в аморфном состоянии больше, чем в кристаллическом. Поэтому аморфные тела могут самопроизвольно переходить в кристаллическое состояние (пример: помутнение со временем стекол).
Кристаллы можно вырастить в домашних условиях.
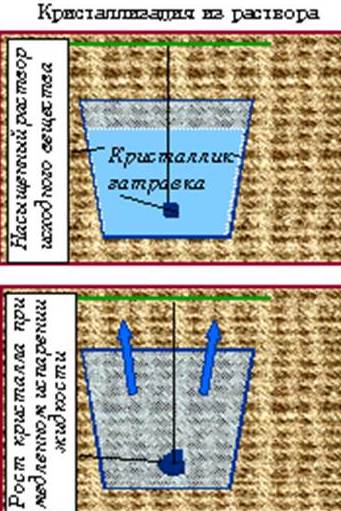 Основные методы искусственного выращивания монокристаллов. Основные методы искусственного выращивания монокристаллов. Существует три способа образования кристаллов: кристаллизация из расплава, из раствора и из газовой фазы. Примером кристаллизации из расплава может служить образование льда из воды (ведь вода – это расплавленный лёд), а также образования вулканических пород.
Пример кристаллизации из раствора в природе – выпадение сотен миллионов тонн соли из морской воды. При охлаждении газа (или пара) электрические силы притяжения объединяют атомы или молекулы в кристаллическое твёрдое вещество – так образуются снежинки.
Наиболее распространёнными способами искусственного выращивания монокристаллов являются кристаллизация из раствора и из расплава
В первом случае кристаллы растут из насыщенного раствора при медленном испарении растворителя или при медленном понижении температуры. Такой процесс можно продемонстрировать в лаборатории с водным раствором поваренной соли. Если дать воде возможность медленно испаряться, то в конце концов раствор станет насыщенным, и дальнейшее испарение приведёт к выпадению соли. Если твёрдое вещество нагреть, оно перейдёт в жидкое состояние – расплав. Трудности выращивания монокристаллов из расплавов связаны с высокой температурой плавления. Например, для получения кристалла рубина нужно расплавить порошок оксида алюминия, а для этого его нужно нагреть до температуры 2030°С. Порошок высыпают тонкой струйкой в кислородно-водородное пламя, где он плавится и каплями падает на стержень из тугоплавкого материала. На этом стержне постепенно и вырастает монокристалл рубина.
Есть кристаллизация из газа.
Понятие о жидких кристаллах .
 Большинство веществ находится в кристаллическое состояние, молекулы образуют трехмерную кристаллическую решетку, упорядоченную в трех измерениях, а при нагревании до определенной температуры наблюдается фазовый переход из трехмерного упорядоченного состояния в разупорядоченное жидкое состояние, при дальнейшем нагревании - в газообразное состояние. Большинство веществ находится в кристаллическое состояние, молекулы образуют трехмерную кристаллическую решетку, упорядоченную в трех измерениях, а при нагревании до определенной температуры наблюдается фазовый переход из трехмерного упорядоченного состояния в разупорядоченное жидкое состояние, при дальнейшем нагревании - в газообразное состояние. Выяснилось, что существуют некоторые промежуточные фазы, которые наблюдаются в агрегатным состоянием жидкости, но, тем не менее, имеют некоторый порядок: не трехмерный, а двумерный или какой-то другой выраженный порядок.
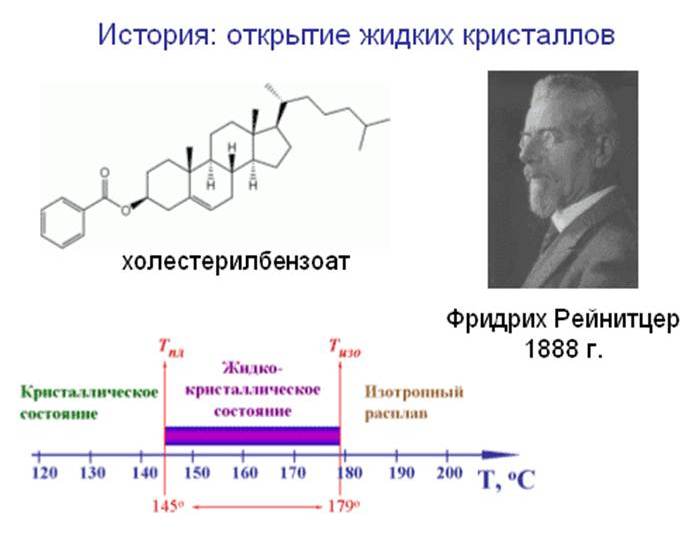
Первое сообщение о необычном состоянии вещества - о жидкокристаллическом состоянии вещества, тогда, правда, этого термина не было, - упоминается в 1888 году. По некоторым другим данным, такое необычное состояние вещества фиксировалось и в 1850 году, но принято считать, что в 1888 году Фридрих Рейницер, австрийский ученый, исследовал вещество холестерилбензоат – и обнаружил, что при нагревании до 145° кристаллическая фаза (белый порошок) переходит в странную мутную жидкость, а при дальнейшем нагревании до 179° наблюдается переход в обычную прозрачную жидкость В 1888 году Рейницер написал, что существуют кристаллы, мягкость которых такова, что позволяет назвать их жидкими, затем Леман написал статью о текучих кристаллах, фактически он придумал термин жидкие кристаллы.
Важный исторический эпизод: в 20-30-х годах советский физик Фредерикс изучал влияние различных полей магнитного и электрического на оптические свойства жидких кристаллов, и он обнаружил важную вещь, что ориентация молекул в жидких кристаллах очень легко меняется под действием внешних полей, причем поля эти очень слабые и изменения очень быстрые.
С конца 60-х годов начался бум изучения жидкокристаллических систем, жидкокристаллических фаз, и он связан с тем, что научились их использовать. Вначале для систем отображения информации в обычных электронных цифровых часах, затем - в калькуляторах, а с появлением компьютерной техники стало понятно, что жидкие кристаллы можно активно использовать для изготовления дисплеев. Естественно, такой технологический скачок стимулировал изучение жидких кристаллов.
 Следует отметить, какой большой временной разрыв между научными открытиями, связанными с жидкими кристаллами. Фактически люди интересовались ими из любопытства, никто не знал, как их использовать. Прошло фактически 80 лет после открытия жидких кристаллов, пока их научились использовать. Следует отметить, какой большой временной разрыв между научными открытиями, связанными с жидкими кристаллами. Фактически люди интересовались ими из любопытства, никто не знал, как их использовать. Прошло фактически 80 лет после открытия жидких кристаллов, пока их научились использовать. Устройство мезофазы или жидкокристаллической фазы.
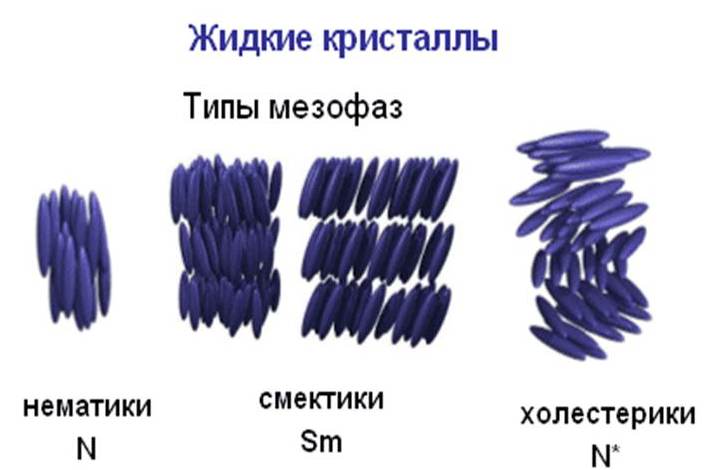
Обычно жидкокристаллическую фазу образуют молекулы, имеющие палочкообразную или дискообразную форму, то есть они обладают анизометрией формы прежде всего - палочки или диски. Можно представить эксперимент, который легко поставить: если насыпать в коробочку палочек хаотично и потрясти, то в результате этого встряхивания мы заметим, что палочки сами по себе уложились параллельно, так и устроена самая простая нематическая фаза. Существуют более сложные фазы, например смектического типа, когда центр масс находится в плоскостях, то есть такие слоистые фазы
Каждый из нас носит с собой небольшое количество жидких кристаллов, потому что все мониторы мобильных телефонов на жидких кристаллах, уже не говорим о мониторах компьютеров, о дисплеях, о телевизионных мониторах, и серьезной конкуренции со стороны плазменных мониторов и мониторов на светодиодах в общем-то нет.
Жидкие кристаллы стабильны, не требуется большого напряжения для переключения картинки – это очень важно.
 В жидких кристаллах наблюдается, так называемая анизотропия свойств, то есть это неодинаковость свойств по различным направлениям в среде, низкая вязкость их, иными словами, текучесть, существует возможность создать какое-то оптическое устройство, которое бы переключалось, реагировало с характерным временем переключения миллисекунды или даже микросекунды - это когда глаз не замечает скорости этого изменения, поэтому и возможно существование ЖК-дисплеев и телевизионных дисплеев, и очень высокая чувствительность к внешним полям. В жидких кристаллах наблюдается, так называемая анизотропия свойств, то есть это неодинаковость свойств по различным направлениям в среде, низкая вязкость их, иными словами, текучесть, существует возможность создать какое-то оптическое устройство, которое бы переключалось, реагировало с характерным временем переключения миллисекунды или даже микросекунды - это когда глаз не замечает скорости этого изменения, поэтому и возможно существование ЖК-дисплеев и телевизионных дисплеев, и очень высокая чувствительность к внешним полям.
 Драгоценные камни служили мерой богатств князей и императоров. Драгоценные камни служили мерой богатств князей и императоров. Иноземные послы, побывавшие в XVII в. в России, писали, что ими овладел «тихий ужас» при виде роскошных нарядов царской семьи, сплошь унизанных драгоценными камнями.
На голове царицы Ирины Годуновой была корона, «как стена с зубцами», разделенная на 12 башенок, искусно выделанных из рубинов, топазов, алмазов и «скатных жемчугов», кругом корона была унизана огромными аметистами и сапфирами.
Митра. Жемчуг Бриллиант «Орлов» в императорском скипетре
Известно, что шляпа князя Потемкина Таврического так была усеяна бриллиантами и из-за этого столь тяжела, что владелец не мог носить ее на голове; адъютант нес шляпу в руках за князем. На одном из платьев императрицы Елизаветы было нашито столько драгоценных камней, что она, не выдержав их тяжести, упала на балу в обморок. Впрочем, еще раньше с супругой царя Александра Михайловича случилось более досадное происшествие: ей пришлось прервать обряд венчания, чтобы снять с себя усыпанный самоцветами наряд.
Самые большие в мире алмазы известны каждый под своим названием: «Орлов», «Шах», «Конкур», «Регент» и др.
|